承载全人类希望的新冠疫苗即将面市,它将对我们的世界做出怎样的贡献?
Gaurav Agrawal、Michael Conway、Jennifer Heller、Adam Sabow、Gila Tolub
全球正在以前所未有的速度和力度研发新冠疫苗(此前研发速度最快的腮腺炎疫苗用时4年)。目前候选新冠疫苗超过250个,其中30个已进入临床试验阶段,约25个有望在今年进入人体试验阶段。预计疫苗将会在2020年第四季度至2021年第一季度间上市,大概率会首先给特定人群接种。至2021年底,会有更多候选疫苗相继面市。
那么,新冠疫苗能否研制成功?如果能,要等到什么时候?疫苗对社会的贡献将有多大?为了弄清这些问题,我们对新冠疫苗研发管线以及潜在情景展开了深度评估。本文初衷并非评判疫苗研发是否应该加速,而是希望表明,在整个疫苗研发过程中严格遵循安全规程,并对结果进行严密监控,才是最重要的。
以下是我们总结的关键信息:
- 候选疫苗有望在2020年第四季度至2021年第一季度间上市,并投入紧急使用。
- 一期和二期临床试验验证了疫苗的安全性和免疫原性,尽管迄今为止受试者数量仍较有限。
- 根据历史成功率推算,基于全球目前的研发管线,至少有7个疫苗有望在未来几年中获得审批。
- 疫苗研发仍面临着诸多挑战,包括验证新的技术平台、确认候选疫苗有足够的防护作用,以及设计最高效疫苗的“脸谱”。
- 监管机构仍在完善新冠疫苗的审批准则。例如,美国食品药品监督管理局称,获得紧急使用授权(Emergency Use Authorization,EUA)之前需要更多数据。
- 疫苗产商已宣布,至2020年底,累计产能可达10亿剂,2021年底可达90亿剂。
新冠疫苗最终将在全球抗疫中扮演何种角色取决于许多因素,如新冠肺炎的流行病学特征和传染性、自然免疫持续时长、疫苗特性以及补充性治疗手段的可及性等。但各界普遍认为,疫苗会在大多数假设情景中扮演重要角色,在更糟糕的假设情景下有可能“拯救世界”。无论如何,疫苗都将成为一道屏障,阻止病毒对人类健康和全球经济造成持续冲击。
有鉴于此,我们建议,疫苗生态系统的参与者应采取下列6项关键行动,提前做好准备:
一是制定预案,力图适应各种需求情景;
二是互通有无,保持疫苗生产灵活机动;
三是取长补短,确保多款疫苗形成互补;
四是通力合作,协同配送、接种和监测;
五是周密布局,提前做好相关配套支持;
六是合理决策,充分考虑疫情后续演变。
时间问题:新冠疫苗何时面世?
随着候选疫苗纷纷进入临床试验阶段,专家们提出了许多时间表。下文将逐一阐述已公布的疫苗时间表信息、一期和二期临床试验中令人鼓舞的早期证据,以及其他几项与病毒特性和创新相关的研发因素。
研发机构和政府官员公布的时间表
美国的第一款疫苗很可能于2020年第四季度至2021年第一季度间上市,2021年还有更多疫苗可能获得FDA的紧急使用授权。中国和欧洲企业也在寻求获得类似的许可(见图1)。
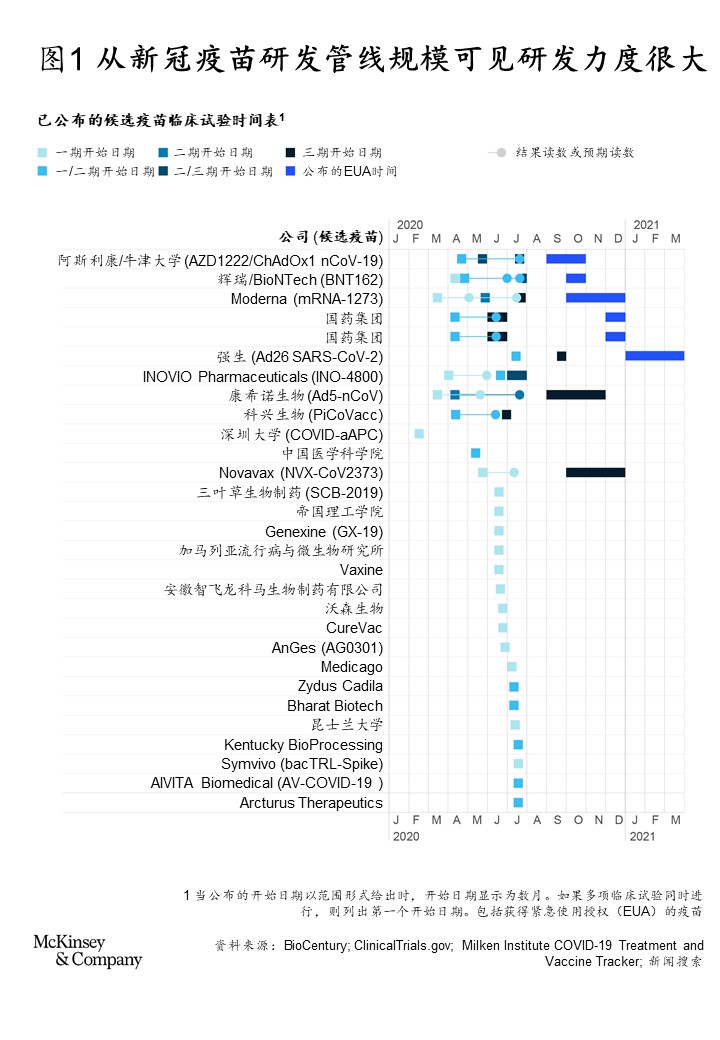
一期或二期临床试验的早期证据
近期,陆续有几家公司公布了一期或二期临床试验的数据。虽然需要更多数据的支撑,但初步结果表明,候选疫苗都能在一定程度上产生中和抗体,这是疫苗有效性的一项潜在指标。
新冠疫苗研发加速推进的因素
进一步审视三大关键研发要素(新冠病毒的基本特征、规模空前的疫苗研发管线和种类多样的技术平台、极为充沛的资金投入),会发现新冠疫苗的研发和审批有望走上“快车道”,超过历史上任何一种疫苗。
- 病毒特征
不同于艾滋病病毒或季节性流感病毒,冠状病毒整体变异速度处于中低水平。早期数据表明,新冠病毒的变异速度仅为季节性流感病毒的1/4。有少量证据表明,变异正在影响新冠肺炎的传播,但迄今为止,其对抗原性的影响似乎微乎其微。这一变异模式对于疫苗研发是有利的,因为不必追随不断变化的靶标去设计疫苗。
- 研发管线和技术平台
新冠疫苗的研发进展神速。在病毒基因测序完成42天后,即诞生了首款候选疫苗。此外,这些候选疫苗采用了多种相关技术,既有蛋白质亚基和病毒载体等成熟的疫苗平台,也包括mRNA和DNA等新型技术平台(见图2)。
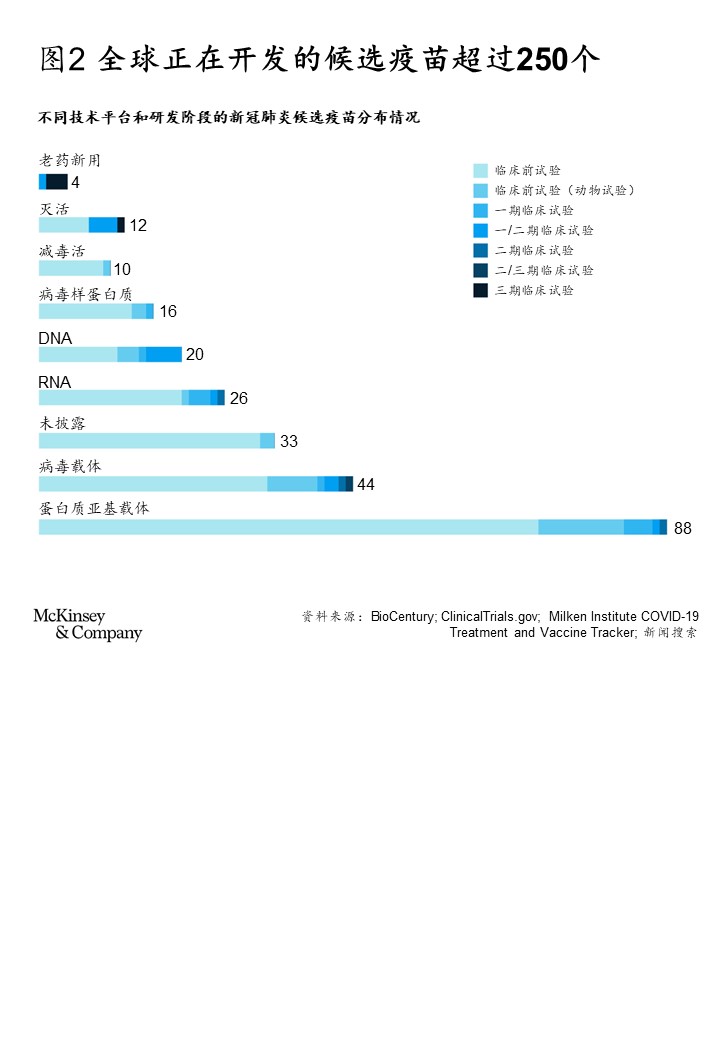
我们对公布的所有候选疫苗进行了分析,基于现有研发管线规模和历史成功率,预计未来两年,约有7~9个疫苗有望通过监管审批。在更加乐观的情况下(如新技术平台的成功率和成熟平台相近,第一批疫苗上市后仍有源源不断的研发),可能超过20个。
3,资金渠道
相比此前的任何一种疫苗,不论是在正常情况下研发的,还是在全球性大流行情况下,新冠疫苗获得的研发资金都更多。迄今为止,全世界对新冠疫苗的总投资至少有67亿美元。公开数据显示,2003~2014年,美国国家过敏症与传染病研究所共计投入2.21亿美元,用于研发埃博拉疫苗。而该研究所在2020年前6个月获得的新冠疫苗研发资金高达15亿美元。
潜在挑战
新冠疫苗的研发有诸多困难需要克服,我们的研究指出了三项关键挑战:验证新的技术平台、证明候选疫苗的防护效果以及设计最高效疫苗的“脸谱”。
— 验证新的技术平台
相较于传统平台,研发新冠候选疫苗时使用的某些技术(如DNA和mRNA)具备独特优势,其中最主要的一点就在于能够加快研发速度。但大都未经验证:使用这些技术研发的人用疫苗,目前尚未出现通过审批的先例。其长期安全性如何,以及能在多大程度上诱发强效而持久的免疫反应,目前仍然存疑。
— 证明候选疫苗的防护效果
疫苗在上市之前,研发机构都需要证明它能有效抵御新冠病毒。有了相关证据后,监管机构才能对该候选疫苗抱有信心,才有可能让高危人群优先接种。疫苗研发机构需要尽可能充实其防护指标。例如,证明该候选疫苗能在接种个体中激发特定水平的抗体反应,以及独立展示抗体在测试或动物模型中能在一定时间段内防止被病毒感染。此外,新冠疫苗研发机构在设计和开展后期临床试验时,还要快速证明其候选疫苗的真实有效性。
—设计最高效疫苗的“脸谱”
研发机构仍面临众多悬而未决的问题,其中之一就是不确定病毒的刺突蛋白将出现多大程度的变异。虽然新冠病毒迄今为止尚未发生显著变异,但如果刺突蛋白在未来发生变异,就会影响当前很多研发中候选疫苗的效果,因为大多数候选疫苗在设计时,都将刺突蛋白作为靶标。如果真的发生变异,候选疫苗就需做出调整,这势必会拖慢疫苗上市的进度。
监管考量
监管方一直在斟酌制定合适的准则,用以评估候选疫苗的各项数据。在2020年底之前,应该会有几家研发机构在疫苗安全性和免疫原性方面具备一定规模的数据。鉴于新冠肺炎在总人口中的致死率,2020年收集的临床试验数据是否足以令监管机构同意为特定高危人群接种疫苗,尚不得而知。
产能考量
迄今为止,已有数家疫苗生产商公布了产能计划,预计到2020年底,新冠疫苗总产能可达10亿剂,到2021年底达到80~90亿剂(见图3)。这一来自行业的数字颇令人鼓舞。只要候选疫苗能通过审批,现在和未来都能有足够的产能满足各类人群的接种需求。
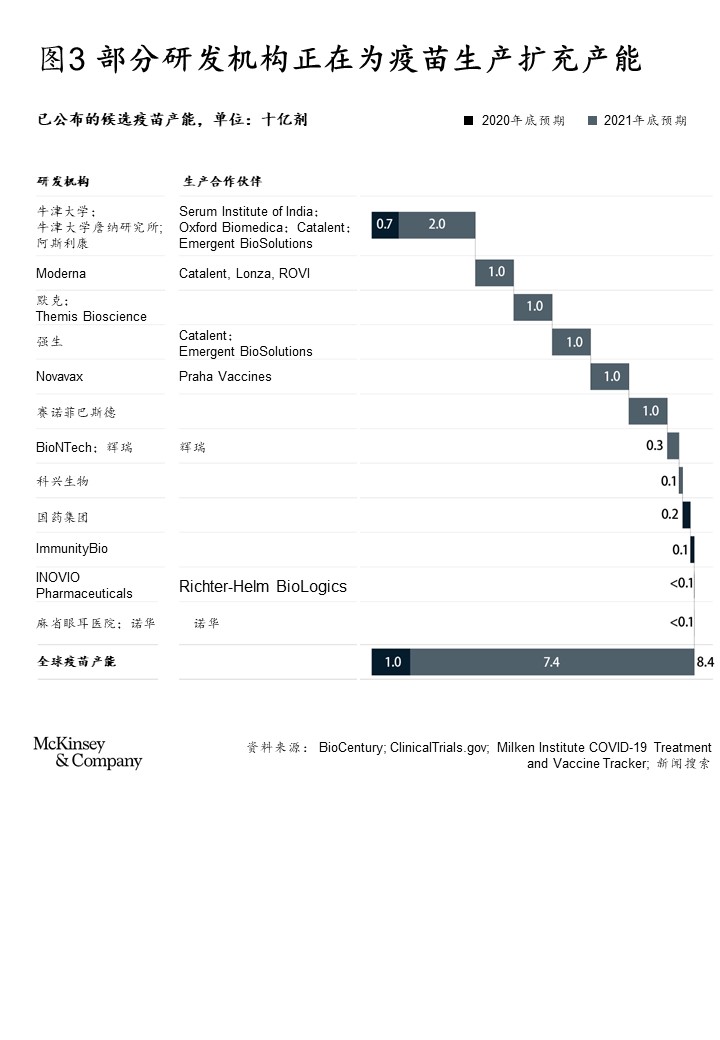
价值问题:疫苗将对社会产生什么影响?
新冠疫苗对人类健康的影响以及对全球经济产生的连带影响将有多大的作用?我们试图从三个不同的时间段来思考这个问题。
在短期内,疫苗可预防更多人被感染和死亡。由此带来的影响包括医疗卫生资源的利用重回可控范畴、形成群体免疫、经济逐步复苏。从中期看,如果疫情转为地方性流行病,有了疫苗,就可让更广泛的人群获得接种(与季节性流感、麻疹、腮腺炎、风疹等其他常规免疫接种类似)。从长期看,如果病毒发生变异,或免疫效果持续时间较短,则可利用当前建立的额外研发能力和产能,快速扩充疫苗供应,或研发新疫苗,并能在未来再次出现全球性大流行病时快速响应(见图4)。

疫苗的社会价值
从短期来看,新冠疫苗的社会价值由4项因素决定:疫苗特性、疾病感染率、自然免疫持续时长、补充性治疗和检测手段,详见下图。

短期疫苗需求
综合考虑所有的价值决定因素后,疫苗的短期需求有多大?我们的研究展示了三种可能情景。
情景一:需求最高。人们将疫苗视为解决新冠危机的关键因素。这一情景表现为:病毒保持中等传播强度,免疫时长有限(自然免疫或疫苗免疫均如此),几乎没有有效治疗方案,而疫苗各方面表现理想,成为抵御新冠肺炎的中流砥柱。
情景二:需求居中。如果传染率保持稳定,疫苗的免疫时长约3~5年,有多种治疗方案,检测能力也有所提升,那么对疫苗的需求就会缓和很多。但仍需用疫苗保护易感群体(如医疗工作者和免疫功能受损的病人),并用于在下一波暴发中的潜在热点地区提前防范。
情景三:传染性减弱,且出现突破性治疗方案。这时疫苗的作用就会比较有限,更多的是作为一种社会保障措施而存在。这种情形下,对疫苗的需求可能更有侧重(例如,专门供高危人群接种),但为研发和扩大新冠肺炎疫苗产能而进行的投资,会更倾向于是对更严重疫情暴发的防范。
备战问题
专家普遍认为,第一款新冠疫苗极有可能在未来6~12个月面市,这对全世界的人民、经济和医疗系统而言不啻为福音。疫苗生态系统的各利益相关方在继续推进研发、生产、政策制定、实施和其他工作时,应采取以下6项行动。
- 制定预案,力图适应各种需求情景
不同情景对疫苗的需求可能不尽相同。政府、物流商、制造商、监管机构和其他相关方都应制定应急计划,除了考虑上文提到的三种情景,还应考虑可能获批的候选疫苗,及其相应的配送与接种要求。
2.互通有无,保持疫苗生产灵活机动
研发机构和投资合作方需共同打造灵活、机动的生产流程和网络。企业还应制定预案,如何在必要时将产能(自身内部产能及通过双边合作获得的外部产能)转移给其他前景更好的疫苗。研发机构必须对新型合作关系持开放态度,在某些情况下甚至要与竞争对手建立合作。除了依靠私营制造企业,现在还出现了公对公合作,进一步扩大产能,拓展全球疫苗的供给渠道。
3.取长补短,确保多款疫苗形成互补
在未来6~24个月内,不同阶段将有不同的疫苗面市、扩产。专家一致认为,包括最早一批疫苗在内,不太可能有哪一款疫苗具备理想疫苗的所有特征,所以卫生官员、政策制定者和监管机构都需谨慎思考,如何运用多款研发中的疫苗打出一套“组合拳”,形成疫苗互补。
4.通力合作,协同配送、接种和监测
科学家在设计、研发、测试和生产安全有效的疫苗方面经验丰富,但如果不能妥善运输、配送和接种疫苗,他们的努力就会付之东流。多个组织已经在确立相应的工作框架,以确保全世界人民都能获得疫苗,这是重中之重。在大多数需求场景下,疫苗供应的速度和规模(可能高达数十亿剂)都是前所未有的。各利益相关方必须站在端到端的视角来定义自身角色,即从产品运输到医疗服务机构咨询,再到疫苗接种,整个过程都要考虑在内。
不同疫苗有不同的配送需求,包括接种剂量、接种地点和冷链要求等。例如,DNA疫苗一般都能常温储存,而RNA疫苗、蛋白质亚基和病毒载体疫苗则需要冷链运输。与疫苗制造一样,各利益相关方应该与合作伙伴一道,根据不同的需求情景制定相应的应急物流计划。比方说,考虑个体接种疫苗的方式,并由此推演应该采取的措施;例如,某疫苗可否就在药房由执业护士实施接种,还是必须要去医院或诊所?
5.周密布局,提前做好相关配套支持
各利益相关方应为疫苗接种提供关键的基础设施。例如,保险公司需要解决最弱势群体的承保问题,限制自费部分支出等,让全世界人民都能用得起疫苗。医疗机构和政府部门可能还需加大科普宣传力度,以增强公众对疫苗的信任。最近的民意调查显示,即使疫苗能在短期内上市,美国也只有约30%的人愿意接种。
6.合理决策,充分考虑疫情后续演变
应以长远眼光看待研发管线中的每一个候选疫苗,考虑当前的决策会如何影响疫苗在大流行过后的现实意义,尤其是考虑到新冠肺炎可能在某些国家/地区转为地方性流行病。这么做除了能确保目前的做法在未来仍有其意义,还很可能进一步彰显为更广泛疫情备战的涓滴效应。
破晓在即,新冠疫苗面市的时间越来越明朗,在全球成功推出有效疫苗所能创造的价值,也越发明确。在大多数情形下,疫苗都将是确保更广大人群获得免疫的重要手段。至少,持续投资于疫苗研发,仍可为人类社会保驾护航,加速步入疫后新常态。从长远来看,研发新冠疫苗的经验教训也是一笔宝贵的财富,可在未来加快其他疫苗的研发速度。
注:限于篇幅,本精简版略去引用的注释。如欲了解更多,请点击此处下载完整版。
作者:
Gaurav Agrawal是麦肯锡全球董事合伙人,常驻纽约分公司;
Michael Conway是麦肯锡全球资深董事合伙人,常驻费城分公司;
Jennifer Heller是麦肯锡全球副董事合伙人,常驻芝加哥分公司;
Adam Sabow是麦肯锡全球资深董事合伙人,常驻芝加哥分公司;
Gila Tolub是麦肯锡全球董事合伙人,常驻特拉维夫分公司。
麦肯锡全球董事合伙人陈波和中国区副主编林琳承担了中文版的审阅和修订工作,在此一并致谢。





